









準備するもの
【使用器具・薬品】
・ 10%硫酸ナトリウム溶液 150ml(硫酸ナトリウム15gを150mlに溶かす)
・ 鉛筆 2本
・ ペットボトル(200~360ml) 1個
・ ビニールテープ
・ ビーカー(300ml) 1個
・ 針金
・ ガスバーナー
・ 三脚
・ ミノムシクリップ付きの電線 2本
・ 電子オルゴール発光ダイオードあるいは電子オルゴール
・ 乾電池(単1~3) 2本
・ 電池ボックス
【材料の入手】
・硫酸ナトリウム 1,000円/500g
・ 10%硫酸ナトリウム溶液 150ml(硫酸ナトリウム15gを150mlに溶かす)
・ 鉛筆 2本
・ ペットボトル(200~360ml) 1個
・ ビニールテープ
・ ビーカー(300ml) 1個
・ 針金
・ ガスバーナー
・ 三脚
・ ミノムシクリップ付きの電線 2本
・ 電子オルゴール発光ダイオードあるいは電子オルゴール
・ 乾電池(単1~3) 2本
・ 電池ボックス
【材料の入手】
・硫酸ナトリウム 1,000円/500g























実験の手順
-
バーナーで鉛筆を焼いて中の芯を取り出す。(2本作成)
- ペットボトルのキャップに鉛筆の芯が入る程度の穴を開ける。(バーナーで加熱した針金を用いると比較的容易。やけどやケガに注意)
- 芯がペットボトル内に落ちてしまわないように、端を少し残してビニールテープを巻く。
- 鉛筆の芯をフタに通し、2本の芯が平行になるようにビニールテープで固定する。
-
ペットボトルに10%硫酸ナトリウム水溶液を入れ、キャップをし、先端部分にミノムシクリップをつける。
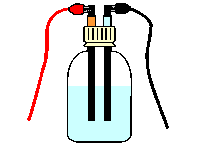
- 鉛筆の芯に繋いでいない方のクリップを乾電池(1.5V以上)につなげ、5分間ほど放置する。
- 十分鉛筆の芯に気泡が溜まったら準備完了。
- 乾電池の+極に付けていたミノムシクリップを発光ダイオードの長い方の足に付けて、-極側を短い方の足につけると発光ダイオードが光る。

アドバイス
- 火気に注意してください。
- 鉛筆の芯はバーナーで焼くと簡単に取り出せます。シャープペンシルの芯でも実験は可能ですが、細く折れやすくので注意してください。
- 硫酸ナトリウム水溶液を電解質溶液に用いましたが、他の電解質溶液でも可能です。水酸化ナトリウムや水酸化カリウムでも可能です。ただし食塩水(塩化ナトリウム水溶液)を用いた場合、塩素が発生しますので、誤って吸入してしまうことがないように十分注意してください。
- 大勢の前で演示する場合は、発光ダイオードよりも電子オルゴールの方がよく分かると思います。

解説
1.燃料電池とは
化学反応から電気を発生させる電池のひとつであり、水の電気分解の逆反応を用いたものです。
通常の一次電池やバッテリーなどの二次電池と異なり、燃料となる物質を供給し続ければ、電気を発生させ続けることができます。
しかも、反応によって生成するのは水だけなのでクリーンなエネルギーとして注目されています。
とはいうものの、燃料電池の発電実験が初めて成功したのは1839年で、170年以上も前のことです。
2.今回の実験について
燃料電池には電解質を使用することが大切ですので、今回の実験では、10%硫酸ナトリウム溶液を用いました。
充電した燃料電池の酸素極(正極)では、
1/2O2+2H++2e-→H2O の反応が起こり、電子e?を必要とします。
水素極(負極)では、
H2→2H++2e- の反応でe-が生成します。
そのため、両極をつなぐとe-を生成する負極からe?を必要とする正極へe-が移動します。
このことにより、電流が流れ、発光ダイオードが光ります。
なお、充電をしている時の反応は逆反応で、
H2O→1/2O2+H2 となり、
水の電気分解反応ということになります。
- コメント(0件)



































コメント投稿はログインしてから実行してください。
コメント投稿